美国芝加哥大学Luis B. Barreiro研究组在Science发文题为Genetic ancestry effects on the response to viral infection are pervasive but cell type specific,揭开了不同遗传祖先的人群对于病毒感染的细胞特异性响应。

为了破除先前研究的一些局限,作者们将单细胞RNA-seq继续与不同的欧洲与非洲遗传祖先来源的外周血单核细胞(Peripheral blood mononuclear cells,PBMCs)体外甲型流感病毒感染实验相联合(图1)。为了排除潜在的特异性表达差异,所以作者们将目标集中在男性中。在病毒感染6小时后,作者们对所有的样品进行了单细胞测序。作者们总共得到了255,731个细胞的转录图谱,同时作者们也对所有个体进行了全基因组测序。通过对外周血单核细胞中的细胞进行聚类,作者们总共揭示出8种不同的细胞类型,其中最主要的有五种细胞,分别是CD4+T细胞、CD8+T细胞、B细胞、自然杀伤细胞以及单核白细胞。其中单核白细胞对于甲型流感病毒的感染具有最强的响应,同时单核白细胞中也表现出胞内最高水平的IAV转录。该结果说明外周血细胞中单核白细胞对于病毒感染是最敏感的,这与前人的研究一致【3】。
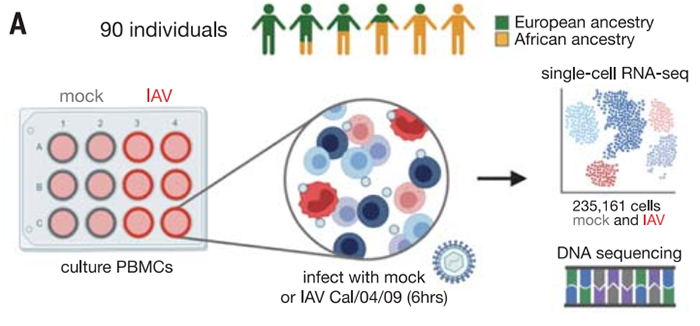
图1 工作流程
进一步地,为了对细胞类型特异性与共性的响应进行剖析,作者们构建了一个基于所有基因在所有细胞中表达差异的“特异性指数”(Specificity score)。作者们发现具有高细胞特异性响应模式的基因主要富集在转录起始以及病毒基因表达中。相反,与I型干扰素信号通路以及响应相关的基因的具有较低的细胞类型特异性。该结果说明I型干扰素信号通路相关的基因是跨不同免疫细胞类型共同的、基础的抗病毒反应。
随后,作者们想鉴定出在基线水平以及在感染后不同遗传祖先群体相关的差异表达基因(Population differentially expressed,popDE)。在不同的感染状况以及不同的细胞类型中,作者们共鉴定出1949个popDE基因,而且遗传祖先对于基因表达的影响是高度细胞特异性的。
为了对该工作的功能性结果进行验证,作者们对10个具有I型和II型干扰素转录水平最强反应性与10个最弱反应性的个体的外周血单核红细胞甲型流感疫苗感染6小时后的分泌细胞因子进行鉴定。高反应性个体在感染后分泌IFN-α2与IFN-β显著高于低反应性个体,而早期诱导出的I型干扰素的响应与晚期病毒低滴度相关,说明早期诱导的免疫细胞反应会降低病毒的感染。为了评估祖先来源不同的遗传变异与病毒感染后的响应之间的关系,作者们对表达数量性状基因座(expression quantitative trait loci,eQTLs)进行寻找,发现在所有细胞类型以及感染状况中有2234个基因具有至少一个顺式eQTLs,也就是单核苷酸多态性。这种顺式调控多态性可以解释遗传祖先相关的基因调控差异。其中最特异的生物信号通路是核糖体蛋白基因表达通路,这对于病毒的转录非常重要。在欧洲血统的个体中,核糖体相关通路的高表达是由影响这些通路中基因调控的顺式调控变异的累积效应驱动的。非洲和欧洲血统个体之间差异表达的基因在与COVID-19严重程度相关的基因中富集存在,这与遗传祖先对观察到的非裔美国人和欧洲裔美国人之间COVID-19易感性差异的潜在贡献相一致。
总的来说,该工作对多种免疫细胞在病毒感染的早期反应的个体差异的基因决定因素进行了描述,扩展了先前对于分离的特定细胞类型的遗传祖先效应的免疫应答影响。欧洲血统的增加与流感感染后较短时间内、较强的I型干扰素反应有关,这使得在较晚时间点病毒滴度降低。该发现不仅对流感病毒的感染具有潜在的临床意义,也对现在SARS-CoV-2病毒的大流行的抗病毒反应时间和大小以及与疾病进展、严重程度的相关性提供了新的思考。













